Các em học sinh thân mến, HOCMAI xin gửi tới các em đề cương ôn thi giữa kì 1 Hóa 9. Như các em đã biết, dưới trải nghiệm của cá nhân mình, môn hóa học thực sự là một trở ngại lớn đối với các em. Môn hóa có rất nhiều ký tự viết tắt, nhiều công thức, định lý, tính chất của vô vàn các chất. Bài viết dưới đây sẽ tổng hợp kiến thức một nửa kì một môn hóa học dành cho các em học sinh khối 9. HOCMAI mong rằng những kiến thức cô đọng dưới đây sẽ hỗ trợ các em phần nhiều trong bài thi giữa kì một.
Bài viết tham khảo thêm:
- Đề cương ôn thi giữa kì I Ngữ Văn 9
- Đề cương ôn thi giữa kì I Toán 9
- Để cương ôn thi giữa kì I Tiếng Anh 9
I. LÝ THUYẾT
1. OXIT
a) Định nghĩa:
Oxit là hợp chất gồm 2 nguyên tố, trong đó có một nguyên tố là oxi.
Ví dụ: CO, CaO,Na2O, SO2, Fe3O4, P2O5, …
b) Tính chất hóa học:
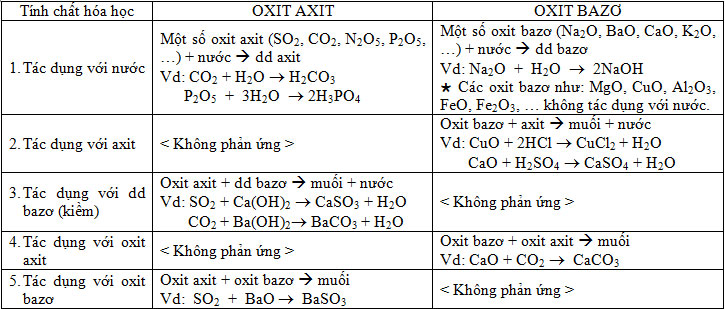
– Oxit lưỡng tính: Oxit lưỡng tính là loại oxit vừa tác dụng dung dịch axit, vừa tác dụng với dung dịch bazơ.
Thí dụ như: ZnO, SnO, Al2O3, Cr2O3,…
Al2O3 + 6HCl → 2AlCl3 + 3H2O
Al2O3 + 2NaOH → H2O + 2NaAlO2 (natri aluminat)
– Oxit trung tính (hay là oxit không tạo muối): Oxit trung tính là oxit không tác dụng với axit, dung dịch, bazơ hay nước như: NO, CO, N2O,…
2. AXIT
a) Định nghĩa:
Axit là hợp chất mà phân tử gồm có một hay nhiều nguyên tử H được liên kết với gốc axit. Các nguyên tử H này có thể được thay thế bằng các nguyên tử kim loại.
Ví dụ: HCl, HNO3, H3PO4, H2SO4,…
b) Tính chất hóa học:
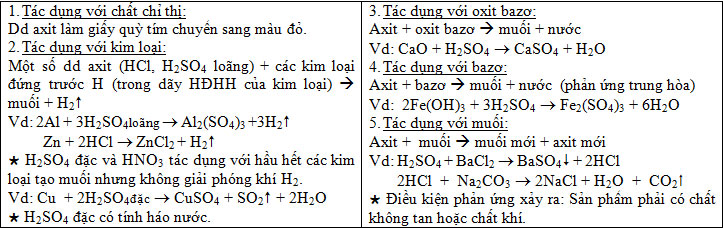
Sản xuất axit sunfuric có những công đoạn như sau:
(1) S + O2 t0,V2O5 → SO2
(2) 2SO2 + O2 → 2SO3
(3) SO3 + H2O → H2SO4
3. BAZƠ
a) Định nghĩa:
Bazơ là hợp chất mà phân tử cấu tạo gồm có một nguyên tử kim loại liên kết với một hay nhiều nhóm hidroxit (OH).
Ví dụ: NaOH, KOH, Ba(OH)2, Al(OH)3, …
b) Tính chất hóa học:
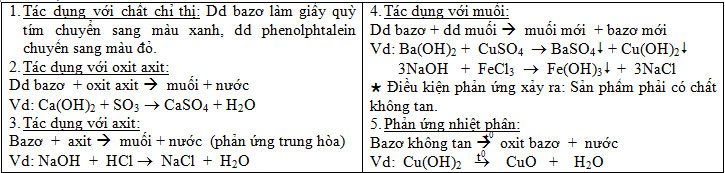
Sản xuất natri hiđroxit:
2NaCl + H2O điện phân dd, có màng ngăn → 2NaOH + Cl2 + H2
- c) Thang pH:
Được dùng để biểu thị độ axit hoặc độ bazơ của một dung dịch:
pH < 7: tính axit; pH = 7: trung tính; pH > 7: tính bazơ
4. MUỐI
a) Định nghĩa:
Muối là hợp chất mà phân tử có một hay nhiều nguyên tử kim loại liên kết được với một hay nhiều gốc axit.
Ví dụ: MgSO4, NaCl, BaCO3, Fe(NO3)2, …
b) Tính chất hóa học:

c) Phản ứng trao đổi:
Là phản ứng hóa học mà trong phản ứng đó hai hợp chất tham gia trao đổi với nhau những thành phần cấu tạo nên chúng để tạo ra những hợp chất mới.
Ví dụ:
BaCl2 + H2SO4 → BaSO4↓ + 2HCl
Na2CO3 + 2HCl → 2NaCl↓ + H2O + CO2↑
CuSO4 + 2NaOH → Cu(OH)2↓ + Na2SO4
NaCl + AgNO3 → AgCl↓ + NaNO3
Điều kiện để phản ứng trao đổi được xảy ra: Phản ứng trao đổi tại bên trong dung dịch của các chất chỉ xảy ra nếu sản phẩm tạo thành có chất khí hoặc chất không thể tan.
Lưu ý: Phản ứng trung hòa cũng là phản ứng trao đổi và luôn luôn xảy ra.
Ví dụ: NaOH + HCl → NaCl + H2O
5. Mối quan hệ giữa những hợp chất vô cơ
Sơ đồ chỉ mối quan hệ giữa các hợp chất vô cơ
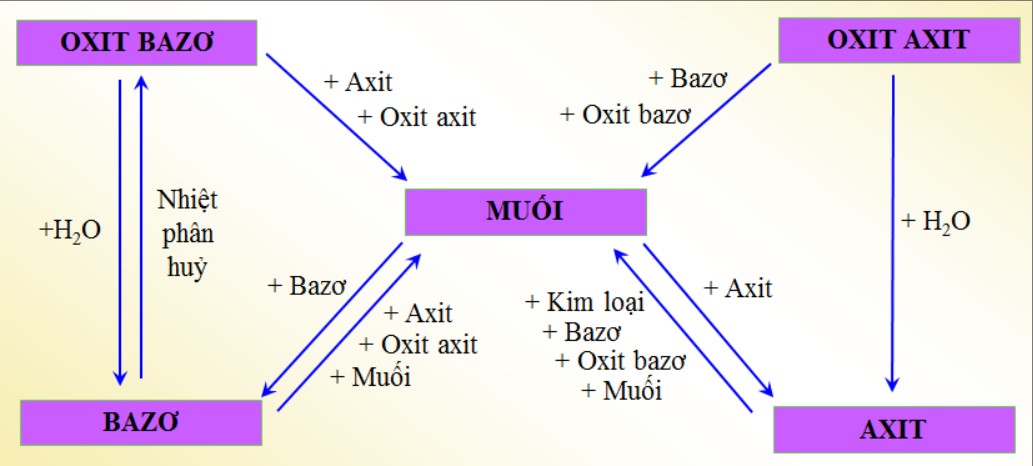
6. Lý thuyết phân bón hóa học
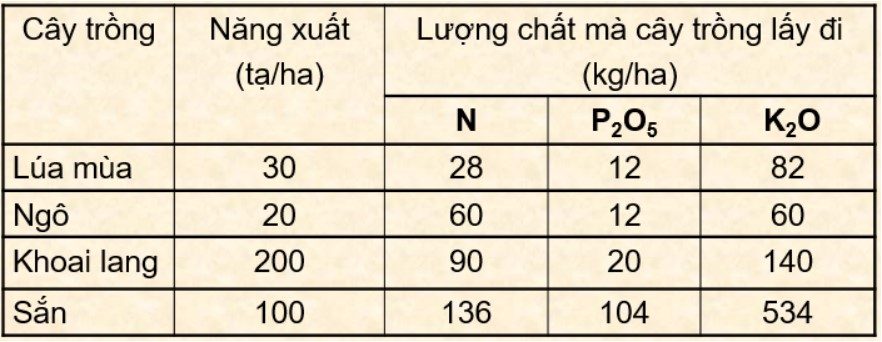
a. Khái niệm
– Phân bón hóa học là hợp chất hóa học chứa nhiều các nguyên tố dinh dưỡng, được bón cho cây nhằm phát triển sự sống của cây, nâng cao năng suất cây trồng.
– Các nguyên tố dinh dưỡng cần cho cây trồng như: B, P, N, K, Ca, Cu, Mg, Zn,…
b. Thành phần của thực vật
– Nước 90%
– Chất khô 10% gồm C, H, O, N, K, Mg, S và các nguyên tố vi lượng B, Cu, Zn, Fe, Mn.
c. Vai trò của các nguyên tố hóa học dành cho thực vật nói chung, cây trồng nói riêng
– Nguyên tố C, H, O: tạo nên gluxit (đường, tinh bột, xenlulozơ) của thực vật trong quá trình quang hợp.
– Nguyên tố N: giúp kích thích cây trồng phát triển mạnh
– Nguyên tố P: giúp kích thích sự phát triển bộ rễ của cây.
– Nguyên tố K: giúp kích thích thực vật ra hoa, làm hạt, tổng hợp nên chất diệp lục.
– Nguyên tố S: giúp cây trồng tổng hợp nên protein.
– Nguyên tố Ca và Mg: giúp cây sinh sản ra chất diệp lục.
– Nguyên tố vi lượng tuy rằng cần thiết cho sự phát triển của thực vật, nhưng dùng thừa hoặc thiếu nguyên tố vi lượng đều sẽ làm ảnh hưởng đến sự phát triển của cây.
II. Bài tập
Câu 1: Có các chất: Al, Fe, MgSO4 ,CuO đựng riêng biệt trong mỗi bình. Cho lần lượt các chất đó vào dung dịch HCl. Số phản ứng xảy ra là:
A.2 B.1
C.3 D.4.
Đáp án chính xác là: C
Câu 2: 0,1 mol AgNO3 được trộn với 0,1 mol HCl, dung dịch được tạo ra sẽ làm quỳ tím đổi sang:
A.màu đỏ B.màu xanh
C.không màu D.màu trắng
Đáp án chính xác là: A
Câu 3: Thể tích khí CO2 bay ra (đktc) khi cho 12,6 gam NaHCO3 tác dụng phản ứng với một lượng dư dung dịch HNO3 là? (H = 1, C = 12, O = 16, Na = 23)
A.3,36 lít B.5,6 lít
C.2,24 lít D.1,12 lít
Đáp án chính xác là: A
Câu 4: Cặp chất nào sau đây sẽ tác dụng với nhau để tạo thành muối kết tủa?
A.Na2O và dung dịch H2SO4
B.CuSO4 và dung dịch BaCl2
C.NaOH và dung dịch H2SO4
D.NaOH và dung dịch BaCl2.
Đáp án chính xác là: B
Câu 5: Để có thể xác minh sự góp mặt của khí SO2 trong một hỗn hợp gồm các khí: SO2, NO, CO ta cho hỗn hợp sục vào nước vôi trong dư, nếu xuất hiện kết tủa trắng thì chứng tỏ trong hỗn hợp đó có góp mặt chất SO2. Em hãy chọn một trong số các chất sau đây để thay cho nước vôi trong (mà vẫn tạo ra kết tủa trắng)
A.dung dịch Ba(OH)2.
B.dung dịch Na2CO3.
C.dung dịch NaOH.
D.dung dịch NaHSO3.
Đáp án chính xác là: A
Câu 6: Các oxit Fe2O3, ZnO, CuO tác dụng được với dung dịch axit vì:
A. đó là những oxit lưỡng tính.
B. chúng không tan trong nước.
C. đó là những oxit có tính bazo.
D. Những oxit này không phải của của kim loại hoạt động mạnh.
Đáp án chính xác là: C
Câu 7: Trong các dãy kim loại dưới đây, dãy nào được sắp xếp đúng theo chiều hoạt động hóa học giảm dần?
A. Al, Fe, Cu, Ag.
B. Cu, Fe, Ag, Al.
C. Ag, Cu, Al, Fe.
D. Fe, Al, Ag, Cu.
Đáp án chính xác là: A
Câu 8: Để trung hòa được 50 gam dung dịch HCl 3,65% cần vừa đủ m gam dung dịch NaOH 4%. Giá trị của m là bằng: (H = 1, Na = 23, Cl = 35,5, O = 16)
A.100 B.75
C.25 D.50
Đáp án chính xác là: D
Câu 9: CaO có thể tác dụng được với CO2 là vì:
A. CO2 là chất khử, còn CaO là chất oxi hóa.
B. CO2 là oxit axit còn CaO là oxit bazo.
C. sẽ tạo ra CaCO3 không tan trong nước.
D. CaO và CO2 đều có thể tan được trong nước.
Đáp án chính xác là: B
Câu 10: Trong một loại oxit sắt, người ta đã xác định được thành phần của sắt theo khối lượng đó là 70%. Công thức của oxit sắt đó sẽ là: (Fe = 56, O = 16)
A. FeO B. Fe2O3
C. Fe3O4 D. Fe2O3 hay Fe3O4.
Đáp án chính xác là: B
Câu 11: Tính chất nào sau đây nói lên được rằng Na có tính kim loại mạnh hơn chất Mg?
- Na cháy được trong không khí, Mg không cháy trong không khí.
- Na tác dụng. Với dung dịch axit, Mg không tác dụng với dung dịch axit.
- Mg thì không tác dụng được với Cl2. Na tác dụng được với Cl2.
- Ở điều kiện thường Na tác dụng được với nước còn Mg thì không.
Đáp án chính xác là: D
Câu 12: Để có thể phản ứng giữa một dung dịch bazơ với dung dịch muối xảy ra thì:
A.chất tạo thành phải không thể tan được trong nước.
B.dung dịch tạo ra bắt buộc phải có pH bé hơn 7.
C.chất tạo thành phải biến đổi quỳ tím thành màu xanh.
D.chất tạo thành không được phép là chất khí.
Đáp án chính xác là: A
Câu 13: lưu huỳnh đioxit được cấu thành từ cặp chất nào sau đây?
A. CaSO3 và HCl
B. CaSO4 và HCl
C. CaSO3 và NaOH
D. CaSO3 và NaCl.
Đáp án chính xác là: A
Câu 14: Để người ta có thể loại bỏ loại bột nhôm lẫn vào loại bột magie bằng cách dùng:
A. dung dịch HCl dư
B. MgCl2 dư.
C. dung dịch NaOH dư.
D. dung dịch CuSO4.
Đáp án chính xác là: C
Câu 15: Dãy chất nào sau đây chỉ gồm có các chất oxit bazơ?
A. CuO, CO, Mg, CaO.
B. CuO, CaO, MgO, Na2O.
C. CaO, CO2, K2O, Na2O.
D. K2O, MnO, FeO, NO.
Đáp án chính xác là: B
Câu 16: Lượng BaO cần đủ cho vào nước để có được 50 gam dung dịch Ba(OH)2 3,42% là (Ba = 137, H = 1, O = 16)
A.2,29 gam B.1,37 gam
C.3,06 gam D.1,53 gam.
Đáp án chính xác là: D
Câu 17: Đơn chất nào sau đây tác dụng với dung dịch H2SO4 loãng và rồi sinh ra chất khí?
A.Cacbon B.Sắt
C.Đồng D.Bạc
Đáp án chính xác là: B
Câu 18. Dãy nào sau đây gồm các chất đều có phản ứng với dung dịch NaOH (dư) tạo sản phẩm chỉ còn là dung dịch không màu?
A. H2SO4, CO2, FeCl2.
B. SO2, CuCl2, HCl.
C. SO2, HCl, NaHCO3.
D. ZnSO4, FeCl3, SO2.
Đáp án chính xác là: C
Bài viết về đề cương ôn thi giữa kì 1 Hóa 9 như vậy đã kết thúc. Các em học sinh đã hiểu hết bài học chưa nhỉ? Môn hóa tuy khó nhưng chỉ cần chăm chỉ cần cù, các em sẽ thấy môn hóa thú vị và dễ hiểu hơn rất nhiều đấy. Các em cũng đừng quên truy cập hoctot.hocmai.vn để tìm thêm những đề cương ôn thi của nhiều môn học cho mình nhé!
















